کل انرژی گرمایی ماده شامل گرمای محسوس و گرمای نهان در دمای مشخص و بر مبنای دمایی از پیش تعریف شده، انتالپی یا برخی اوقات گرمای کل یا محتوای گرمایی خوانده میشود. انتالپی برحسب واحد گرمایی بر واحد وزن برای مواد جامد و مایع با (Btu/1b) یا (kj/kg) و بر واحد حجم برای گازها با (Btu/ft) یا (kj/m) سنجیده میشود. به عنوان مثال انتالپی آب در دمای صفر درجه سلسیوس یا ۳۲ درجه فارنهایت صفر محسوب میشود و مقدار گرمای لازم برای افزایش یک درجه دمای یک واحد جرم آن، یک واحد انرژی گرمایی در نظر گرفته میشود. بنابراین بر مبنای آحاد انگلیسی برای افزایش دمای یک پوند آب، یک انرژی گرمایی مورد نیاز حواهد بود.
فشار
اگر به یک فشارسنج عقربهای که به هیچ کجا نصل نیست نگاه کنیم ،عقربه باید روی صفر باشد؛ اما این به معنای عدم وجود فشار در اطراف ما نیست. بلکه فشاری برابر با ۱۴.۷ پوند بر اینچ مربع یا ۱.۰۱۳۳ بار جیوه بر کلیه اجسام وارد میشود که فشار اتمسفریک یا فشار جو نامیده میشود. فشاری کمتر از این مقدار خلاء محسوب شده و فشاری بیش از آن شرایطی پر فشار تر را نسبت به فشار جو به وجود میآورد.
بنابراین رابطه فشار و حجم یک گاز در شرایط مفروض اولیه با رابطه فشار و حجم همان گاز در شرایط جدید در دمای ثابت برابر است. اما واقعیت دیگری نیز وجود دارد و آن این است که با فشردن گاز حرارت تولید میشود. بنابراین چنانچه بخواهیم فرایند تراکم، ایزوترمال باشد باید به اندازه گرمای تولید شده ، گاز در حال انقباض را سرد کنیم تا دما ثابت باقی بماند.
این مورد در حال انبساط گاز نیز به گونه عکس صادق است . زیرا دمای گاز در حال انبساط کاهش مییابد و در فرایند ایزوترمال باید به اندازه گرمایی که گاز از دست میدهد، آن را گرم کرد تا تغییرات حجم ناشی از فشار در دمای ثابت صورت گیرد و تلاش در جهت ثابت نگه داشتن دما مستلزم انجام کار و صرف انرژی توسط یک عامل دیگر است.

چنانچه سیلندری از گاز داشته باشیم که نسبت به محیط اطراف کاملاً عایق باشد و تراکم در آن بدون اصطکاک پیستون انجام شود؛ عمل انقباض و انبساط گاز توام با افزایش و کاهش گرمایی خواهد بود که به بیرون راهی نخواهد داشت.
به چنین فرایندی که در آن عمل انقباض و انبساط گاز بدون تبادل گرما با فضای بیرون از محفظه یا سیلندر صورت میگیرد، فرایند آدیاباتیک یا بی دررو گفته میشود.
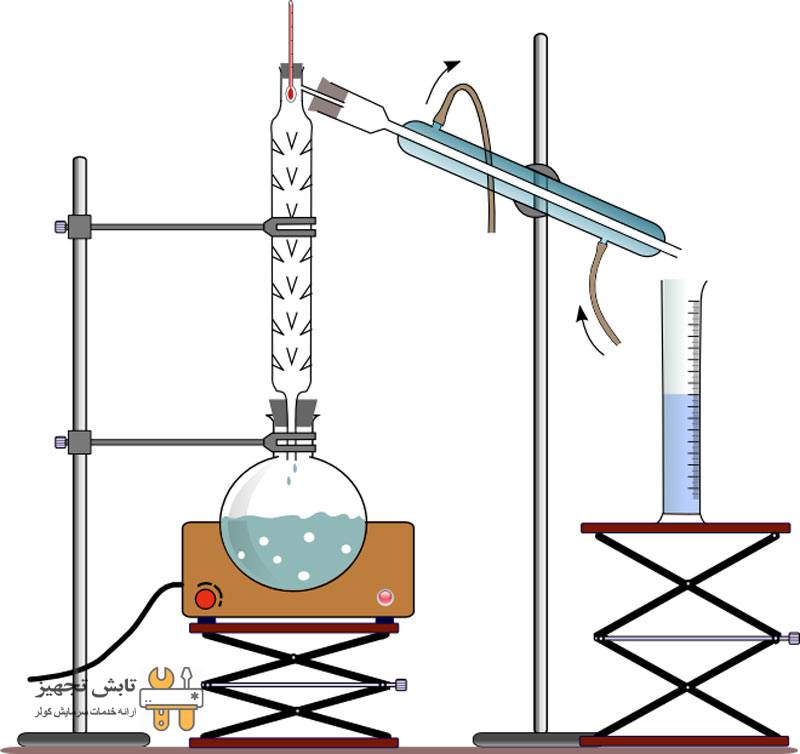
تقطیر و تبخیر
فاصله مولکولی بین گاز ها زیاد و در عین حال فاصله مولکولی مایعات کمتر از گاز ها است و یا به عبارت دیگر جاذبه بین مولکولی گاز ها بسیار کمتر از مایعات است. بنابراین برای تبدیل یک گاز به مایع لازم است که به طریقی فاصله مولکولی آن را کم کنیم.
برای این کار اولین امکانی که به ذهن خطور میکند، فشردن گاز است. در واقع باید با روشی مولکولهای گاز را متراکم و به یکدیگر نزدیک کرد. فشار مکانیکی توام با سرد کردن راهکار بسیار مناسبی برای تبدیل گاز به مایع یا تقطیر است. طبیعی است که برای مایع کردن گاز باید انرژی صرف کرد ؛ اما در مقابل نیز وقتی مایع، تحت فشاری کمتر به گاز تبدیل میشود انرژی گرفته شده را باز پس می دهد . اصولا نقطه جوش هر مایع ای وابسته به فشار است. با افزایش فشار دمای جوش بالا رفته و تبخیر آن به تاخیر میافتد.
گازی که با اعمال فشاری بیش از فغشار جو تبدیل به مایع می شود تا زمانی در حالت مایع میماند که فشار کاهش نیابد. در غیر این صورت ماده به شکل اولیه خود در حالت طبیعی در می آید و در اینجا منظور ما از حالت طبیعی، شرایط فشار جو و دمای محیط بین ۲۰ تا ۲۵ درجه سلسیوس یا ۶۸ تا ۷۷ درجه فارنهایت است. در هر حال تقطیر، فرایندی گرماده و برعکس آن ، تبدیل مایع به گاز یا همان تبخیر فرایندی گرماگیر است. بنابراین اگر ماده ای که تحت فشاری بیش از فشار جو تبدیل به مایع شده است دچار کاهش فشار شود، تبخیر شده و گرمای لازم برای این تغییر حالت را از محیط اطراف میگیرد.
به عنوان مثال نیتروژن مایع در دمای (۳۲۰-) درجه فارنهایت یا (۱۹۵-) درجه سلسیوس در فشار جو تبخیر میشود. بنابر این برای نگه داری آن به صورت مایع لازم است که آن را در کپسولی تحت فشار ۲۰۰ پوند بر اینچ مربع قرار دارد . چنانچه شیر کپسول حاوی نیتروژن مایع باز شود، فشار داخل کپسول کاهش یافته و نیتروژن به سرعت تبدیل به بخار شده و گرمای بسیار زیادی را از محیط اطراف گرفته و یا به عبارت دیگر سرمای بسیار شدیدی تولید میکند. نقطه جوش بسیار پائین نیتروژن در فشار جو، آن را در گروه مبردهایی با قابلیت تولید سرمای زیاد یا کریوژنیک قرار میدهد.
بنابراین می توان از نیترژن مایع برای رسیدن به دماهای کم تا ۲۰- درجه فارنهایت یا حتی کمتر استفاده کرد. اما در چیلرهای تراکمی که قرار است دمای آب را حداکثر تا ۷ درجه سلسیوس برای تامین سرمایش ساختمان و تهویه مطبوع پائین بیاورند نیازی به استفاده از مبردهای کریوژنیک نیست، بلکه از مبرد های دیگری استفاده میشود.
شرایط عمومی راهبری چیلر تراکمی
شرایط استاندارد برای چیلر های تراکمی به قرار زیر است:
- دمای آب سرد خروجی از چیلر
- دبی آب سرد
- دمای آب ورودی به کندانسور
- دبی آب کندانسور
- ضریب رسوب گذاری اوپراتور و کندانسور
اصول ترمودینامیکی سرمایش تراکمی
تبدیل انرژی به ویژه انرژی گرمایی و نسبت آن با حالت مواد، شاکله اصلی مباحث ترمودینامیکی است. در واقع ترمودینامیک، کنش مکانیکی حاصل از گرما است. از این رو موضوعات مرتبط با سرمایش و یا به عبارت دیگر کاهش گرما هم، بر پایه قواعد ترمودینامیک تحلیل میشوند.
کارشناس تعمیر کولر گازی در اصفهان با تسلط بر مفاهیم فوق اقدامات لازم برای تشخیص آسیب را انجام میدهد.



 شرکت تابش تجهیز ارائه دهنده خدمات سرمایش اسپلیت و داکت اسپلیت با 10 سال سابقه کار و فعالیت.
شرکت تابش تجهیز ارائه دهنده خدمات سرمایش اسپلیت و داکت اسپلیت با 10 سال سابقه کار و فعالیت.







دیدگاه خود را ثبت کنید
میخواهید به بحث بپیوندید؟مشارکت رایگان.